Гетерогенный катализ играет огромную роль во многих природных и технологических процессах. В наше время в качестве катализаторов все шире применяются наночастицы. Из-за высокоразвитой поверхности они и так превосходят по своим каталитическим свойствам объемный материал. Но часто (например, для золота) каталитическая активность резко увеличивается по совершенно другим причинам, таким как изменение структуры энергетических уровней по сравнению с объемным образцом. Многие из катализируемых реакций являются эндотермическими, так что актуален вопрос подвода тепла. Он, разумеется, может осуществляться множеством, как простых, так и весьма экзотических, методов. Об одном из них хотелось бы рассказать поподробнее.
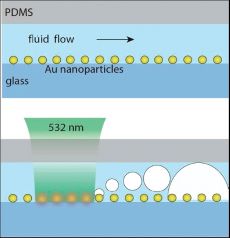
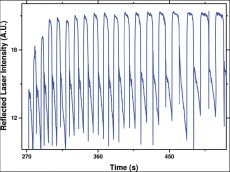
Так как катализируемая реакция протекает на поверхности наночастиц, то логично подогревать именно саму наночастицу. Наночастицы золота крепятся на поверхности стекла, погруженного в реакционную смесь. При помощи маломощного лазера в металлических наночастицах наводятся "токи", точечно обогревающие место протекания реакции с помощью Джоулева тепла. Нужно сказать, что электроны частиц благородного металла, используемых для катализа, могут входить в резонанс с видимым светом и запасать таким образом энергию. Потом запасенная энергия быстро конвертируется в тепло, которое передается окружающей частицу жидкости или газу и, в первом случае, формирует небольшой пузырек газа, катализ в котором более эффективен. Эта технология позволяет строго контролировать количество и место подведения тепла.
В качестве носителя каталитических наночастиц было
предложено воспользоваться капиллярами модифицированного (для лучшего
закрепления наночастиц) стекла. Длина таковых порядка
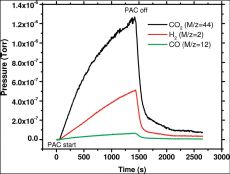
Любопытный факт, что для столь малых пузырьков значительно поднимается внутреннее давление. А вследствие этого растет температура, необходимая кипения смеси (в описываемом случае - примерно на 108 К). Повышение температуры и давления также оказывают положительное влияние на скорость протекания реакции. Основная реакция в данной смеси - каталитический риформинг этанола:
C2H5OH + 3H2O → 2CO2 + 6H2
СО образуется в результате одной из побочных реакций. Предполагается, что дальнейшие исследования в этом направлении помогут добиться практически 100% выхода водорода по этой технологии, а также обеспечить проведение многих других нуждающихся в катализе реакций, имеющих куда большее промышленное значение.